Обеззараживание и обезвреживание с использованием окислителей природных, сточных вод и их осадков
Хлорирование воды порошкообразными хлорсодержащими реагентами и диоксидом хлора.
На малых станциях и водоочистных установках часто целесообразно отказаться от использования жидкого хлора и применять твердые, порошкообразные вещества - хлорную известь и гипохлорит кальция. Эти вещества менее опасны в обращении, процесс их подготовки и подачи значительно проще - практически аналогичен применению коагулянта.
Хлорную известь получают при обработке сухой, негашеной взвести хлором. При контакте с воздухом и влагой хлорная известь постепенно разлагается
2СаС12О+СО2+Н2О ® СаСО3+СаС12+2НС1О
поэтому реагент необходимо хранить в сухом, вентилируемом помещении в закрытой таре.
Гипохлорит кальция образуется при насыщении известкового молока хлором
2Са(ОН)2+2С12 ® Са(С1О)2+СаС12+2Н2О
Товарный продукт СаСl2O или Са(С1O)2 растворяют в растворном баке с механическим перемешиванием. Количество баков не менее двух. Затем раствор разбавляют в расходном баке до концентрации 0,5 . 1% и подают в воду дозаторами растворов и суспензии.
Учитывая коррозионную активность раствора, баки следует изготовлять из дерева, пластмассы или железобетона, из коррозионностойких материалов (полиэтилен или винипласт) должны быть также трубопроводы и арматура.
Диоксид хлора получают непосредственно на водоочистной станции хлорированием хлорита натрия NaС1O2:
2NaClO2 + С12® 2С1O2+2NаС1
Вместо хлора можно для получения ClO2 также использовать озон или сoляную кислоту
2NаС1O2 + O3 + Н2O ® 2С1O2 + 2NаОН+O2;
5NaС1O2+4НС1 ® 4С1O2 + 5NаС1+ 2Н2O,
СlO2 является ядовитым, взрывоопасным газом с интенсивным запахом, водный раствор его практически безопасен. По сравнению с Cl2 двуокись хлора имеет ряд преимуществ - более высокая бактерицидность в щелочной среде, более активно окисляет органические вещества, может разлагать фенолы, не придавая при этом воде хлорфенольного запаха, наличие в воде аммиака не снижает эффективности ClO2.
Хлорирование воды гипохлоритом натрия.
На водоочистных станциях, где суточный расход хлора не превышает 50 кг, где транспортировка, хранение и подготовка токсичного хлора связаны с трудностями, можно для хлорирования воды использовать гипохлорит натрия NаСlO. Данный реагент получают на станция в процессе электролиза раствора поваренной соли. Электролизная установка состоит из бака концентрированного раствора соли (растворного бака), электролизной ванны (электролизера), бака-накопителя раствора гипохлорита, выпрямителя и блока управления.
Растворных баков должно быть не менее двух, их суммарный объем должен обеспечить бесперебойную работу установки в течение 24 ч. При мокром хранении соли объем растворных баков принимается из расчета 1,5 м3 на 1 т соли. Допускается хранение соли на складе в сухом виде, причем толщина слоя соли не должна превышать 2 м.
В растворном баке изготовляется раствор, близкий к насыщенному -200 .310 г/л. Для перемешивания применяют механические устройства н циркуляционные насосы.
Электролизеры могут быть проточного или непроточного типа. Наиболее широко используют последние. Они представляют собой ванну с установленным там пакетом пластинчатых электродов. Электроды, как правило графит, присоединяют в сеть постоянного тока.
В электролизной ванне происходит диссоциация соли, a также воды. При включении электролизера в сеть на аноде будет происходить окисление хлоридов 2Сl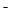 - 2e ® Cl2, затем их гидролиз Сl2 + Н2O ® НС1O+НC1. На катоде выделяется газ Н2, образуется едкий натр
- 2e ® Cl2, затем их гидролиз Сl2 + Н2O ® НС1O+НC1. На катоде выделяется газ Н2, образуется едкий натр
В результате реакции NаОН с НСlO образуется гипохлорит.
В межэлектродном пространстве электролизера непроточного типа плотность электролита в результате его насыщения пузырьками газа будет меньше, чем в остальном объеме ванны, поэтому будет происходить циркуляция раствора - между электродами восходящее, в остальной ванне нисходящее течение электролита. Циркуляция продолжится до полного электролиза всего раствора поваренной соли. Затем электролизная ванна опорожняется и заполняется новой порцией раствора NaCl.
При работе электролизера необходимо свести к минимуму распад образованного NaClO. Для этого следует процесс электролиза проводить при низкой температуре и большой плотности тока на аноде, воздерживаясь от перемешивания электролита в ванне.
Перейти на страницу:
1 2 3 4 5 6 7 8
Интересное по теме
Влияние искусственно вносимой соли NaF на накопление фтора в почве и разнотравье луга )
Развитие любого промышленного производства совсем не
дающего загрязняющих выбросов в окружающую среду не осуществимо не только в
России, но и не в одной стране мира. Поэтому в ближайшем будущем и отдаленной
перспективе проблема загрязнения ...
Природные ресурсы - как основа функционирования мировой экономики
Актуальность темы исследования. Гармоничное
сотрудничество человека с природой, его разумная общественная деятельность,
которая регулирует и контролирует обмен веществ между природой и обществом,
стало в современную эпоху одной из актуальн ...

